이온화 에너지(ionization energy)란 기체 상태의 중성 원자에서 전자 1몰(mol)을 떼어내는 데 필요한 에너지를 말합니다. 이때 전자는 제일 바깥 전자껍질의 전자(최외각 전자)를 말하며 전자는 원자핵과 인력이 작용하기 때문에 이온화 에너지는 양의 값을 갖습니다. 즉 이온화 에너지가 크다는 것은 입자가 전자를 잃기 어렵다는 것을 의미합니다.
원자 번호에 따른 이온화 에너지의 경향성
2, 3주기 원소의 이온화 에너지는 다음과 같습니다.
| 원자 번호 |
원소 | 이온화 에너지 (kJ/mol) |
| 3 | Li | 520 |
| 4 | Be | 900 |
| 5 | B | 800 |
| 6 | C | 1090 |
| 7 | N | 1400 |
| 8 | O | 1310 |
| 9 | F | 1680 |
| 11 | Na | 500 |
| 12 | Mg | 740 |
| 13 | Al | 580 |
| 14 | Si | 790 |
| 15 | P | 1060 |
| 16 | S | 1000 |
| 17 | Cl | 1260 |
이를 그래프로 나타내면 다음과 같습니다.

같은 족에서의 이온화 에너지
같은 족에서는 원자 번호가 커질수록 이온화 에너지가 감소하는 경향을 보입니다. 즉 주기가 증가할수록 전자를 떼어내기가 쉬워지는데요 전자껍질이 증가함에 따라 원자핵과의 인력이 줄어들기 때문입니다.
같은 주기에서의 이온화 에너지
같은 주기에서는 원자 번호가 커질수록 이온화 에너지가 증가하는 경향을 보입니다(물론 예외는 있습니다만). 원자 번호가 증가함에 따라 양성자수가 증가하고 원자가 전자가 느끼는 유효 핵전하가 커집니다. 즉, 원자핵과의 인력이 증가함에 따라 전자를 떼어내는 게 어려워지지요.
유효 핵전하와 가려막기 효과
원자는 원자핵과 전자로 구성되어 있습니다. 원자핵은 양전하(+), 전자는 음전하(-)를 띠고 있지요. 때문에 원자핵과 전자는 서로 인력이 작용하게 되는데요. 원자번호가 커질수록 양성자수가 증
eui232.tistory.com
이온화 에너지 경향성의 예외
대체로 같은 주기에서 원자 번호가 커질수록 이온화 에너지가 증가하지만 경향성에서 벗어나는 부분이 나타납니다. 바로 2족과 13족, 15족과 16족에서 그러한데요. 그 이유는 다음과 같습니다.
2족과 13족 원소의 이온화 에너지 비교
2주기 원소인 Be과 B를 이용하여 설명하겠습니다. 두 원소의 바닥상태 전자 배치를 나타내보면 다음과 같습니다.

전자를 떼어낼 때 Be은 2s 오비탈의 전자를, B는 2p 오비탈의 전자를 떼어내는데요. 에너지가 더 높은 2p 오비탈의 전자가 더 쉽게 떨어지는 것이지요.
15족과 16족 원소의 이온화 에너지 비교
2주기 원소인 N와 O를 이용하여 설명하겠습니다. 두 원소의 바닥상태 전자 배치를 나타내보면 다음과 같습니다.
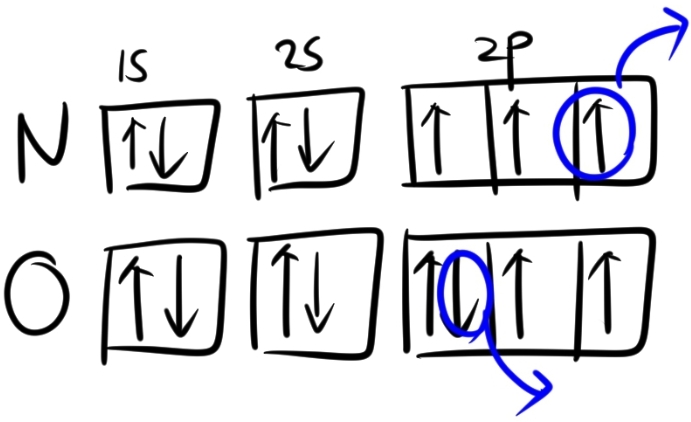
O 원자의 전자를 떼어낼 때 2p오비탈의 짝지어진 상태의 전자를 떼어내는데요. 이때 전자 사이의 반발력이 작용하므로 더 잘 떨어집니다.

'공부합시다 > 화학 이야기' 카테고리의 다른 글
| 분자의 구조, 전자쌍 반발 이론(VSEPR theory) (0) | 2023.07.18 |
|---|---|
| 순차적 이온화에너지의 정의와 크기 비교 (0) | 2023.07.10 |
| 동아리 활동, 간단한 화학 실험, 물의 전기 분해 (0) | 2023.07.06 |
| 오비탈과 양자수의 의미 (0) | 2023.07.03 |
| 원자의 구조와 오비탈의 등장 과정 (0) | 2023.07.03 |



